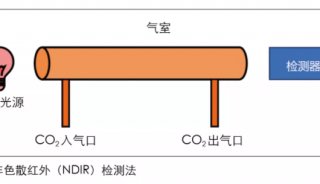
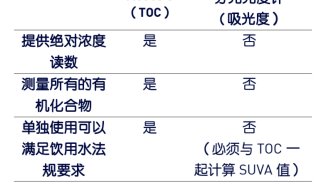
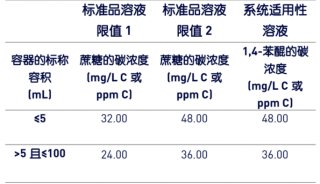
FDA的過程分析技術PAT指南應用于實時檢測RTT

2004年,FDA發布了關于過程分析技術(PAT,Process Analytical Technology)的指導文件。它包含非約束性建議,旨在鼓勵GMP制造商部署PAT以實現過程理解、過程控制和穩健的風險管理。PAT允許實時檢測所需的質量屬性以優化效率。獲得實時數據的眾多好處之一是無需手動采樣或實驗室分析即可理解和演示已驗證的工藝過程狀態。
什么是實時檢測RTT
(Real-Time Testing)?
在其他技術中,GMP制造商通過實施符合ASTM E2656的實時檢測(RTT)來利用PAT,為制藥用水的總有機碳(TOC)檢測提供了標準實踐。在線TOC數據有多種使用方式——過程監控、過程控制和過程理解。RTT經驗證可提供過程監控、過程控制和過程理解,以實時將水放行用于生產。
在考慮將RTT集成到當前制造/生產實踐中時,需要注意以下幾個階段:準備任務、實施程序和持續維護。下面概述了RTT項目各階段的步驟方法,其中包括每個階段成功的關鍵要素。
RTT階段 | RTT要素 |
第1階段 組織和定義 | ★ 確定項目范圍和原則 |
第2階段 風險評估 | ★ 評估當前和未來的階段 ★ 技術選擇 ★ 在水系統中放置未來階段需使用的儀器 |
第3階段 實施 | ★ 驗證未來階段使用的儀器 ★ 方法轉移(從當前到未來階段) ★ 檢測系統等效性 ★ 使用點兼容性研究 |
第4階段 報告/數據處理 | ★ 數據處理和報告工具 ★ 報警和操作限值 |
第5階段 維護 | ★ 災難性故障冗余性 ★ 預防性維護 ★ OOS調查程序 |
第1階段
組織和定義
啟動RTT項目需要團隊、理由和變更控制批準。將質量檢測從實驗室轉移到基層生產車間需要各職能部門的集體努力并達成共識,以建立基于風險的科學策略,從而實施在線TOC以實現水的實時放行。強烈建議來自所有相關職能部門的管理人員加入該團隊,包括:質量保證、質量控制、驗證、制造工程、設施/公用工程、計量和生產。
從第1階段到最終實施,變更控制委員會將參與審查、批準/否決和監控所獲得變更的長期影響。變更控制委員會的職能是在RTT項目的整個過程中確保過程完整性并遵守法規要求。
第2階段
風險評估
在采用任何新技術時,都需要進行風險評估。對于RTT,與該項目相關的兩個主要風險是引入新技術并確保儀器記錄的檢測結果能夠指示水循環沿線的所有使用點(POU)。實施階段包括一項橋接研究和一項POU可比性研究,以說明這些風險。在進行這些研究之前,應進行失敗模式和影響分析(FMEA,Failure Mode and Effects Analysis),以評估過渡到新技術的相關風險,確定儀器記錄的位置,并考慮對水回路中每個POU的風險進行排序。
在準備執行FMEA時,有必要評估將發生變化的當前與未來階段參數——采樣計劃、不合格(OOS)報告、設備地圖、標準操作程序(SOP)、水系統設計、POU關鍵性等。定義這些參數以及它們會發生的變化最終會影響FMEA。
在啟動FMEA時,應考慮將要引入的技術。要過渡到RTT,當前和未來階段的儀器在儀器確認和方法驗證上應該“同等”或“同類”。方法驗證包括準確性、精密度、穩健性、靈敏度、特異性、系統適用性、檢測限和定量限協議,以確定方法是否適合其預期用途。
完成FMEA后,可根據最能反映所有POU的水回路區域確定RTT儀器記錄的位置。當水通過并返回儲罐時,返回儲罐的POU最有可能捕獲和記錄指示所有其他POU的檢測值。有少數例外情況,可能需要第二臺用于RTT的記錄儀器(例如,閉環回路或熱交換器);然而,大多數情況下,返回到儲罐的儀器能準確涵蓋整個水系統。
第3階段
實施
實施階段在RTT流程概述中顯示為淺橙色,因為它是最終用戶可以/可能外包給RTT解決方案提供商的唯一階段。解決方案提供商可能會有一個與實施階段相關的驗證支持包(VSP),其中包含適用于RTT驗證的所有必要的儀器安裝確認(IQ)、運行確認(OQ)和性能確認(PQ)指標。除實施階段外,最終用戶還擁有第1階段(組織和定義)、第2階段(風險評估)、第4階段(報告/數據處理)和第5階段(維護)的要素和可交付成果,使實施階段成為流程的獨特階段。
對于RTT項目,從當前的實驗室取樣實踐階段轉變為未來的在線監測和實時水放行階段,首先需要標準的儀器安裝確認、運行確認和性能確認(IOPQ)來驗證未來階段的儀器。
橋接研究有助于根據ASTM E2656要求,將未來階段與當前階段的性能進行比較,即未來階段儀器必須與當前階段性能“相當或更好”。通過比較當前階段的實驗室儀器與未來階段的在線儀器的性能,橋接研究包括實施階段的方法轉移和方法等效性要素。
最后,風險最高的POU將由FMEA確定,每個POU上的TOC屬性將與永久安裝的記錄儀器進行比較。這樣做,可確保永久安裝的RTT記錄儀器輸出反映水回路中所有POU的檢測值,并完成POU可比性研究。
第4階段
報告/數據處理
21 CFR第11部分是數據可靠性的巔峰之作,適用于制藥、生物技術、化妝品、醫療器械及食品飲料行業。維護受保護的/唯一登錄、控制數據/元數據以及生成審計追蹤只是維護數據可靠性法規的幾種方法。
在RTT情況下,遠程登錄和具有相關審計追蹤的可傳輸數據對于限制直接訪問記錄工具的需求非常有價值。擁有一個具有專業知識的內部IT部門,以這種方式完全依靠SCADA系統路由數據是一種選擇;然而,現在有一些固件和軟件包允許用戶將數據從在線儀器記錄中分離出來,并連接到QC/QA實驗室進行簽核,同時保持必要的審計追蹤,以便于RTT等應用訪問和使用。
設置操作和警報限值也是報告/數據處理階段的關鍵要素。從建立過程能力指數(Cpk)和過程性能指數(Ppk)開始,將提供對工藝性能隨時間變化的統計洞察力。Cpk和Ppk量化了外部限制與過程中心的標準偏差。使用已知的Cpk和Ppk定義操作和警報限值將有助于識別RTT的趨勢,并在違反操作或警報限值的情況下建立程序和響應。
第5階段
維護
對于任何資本支出設備,為實現最佳的儀器壽命,維護是必要的,而且還需要為記錄儀器發生故障的事件做好計劃。對于RTT,應考慮冗余、預防性維護和不合格(OOS)程序。
簡單地維護實驗室實踐(當前階段)SOP可能是一種冗余形式,以防在線記錄儀器出現故障。預防性維護方案應由RTT儀器供應商確定,并且可以安排例行維護訪問。對于實驗室和RTT期間的OOS,FDA的《藥品生產OOS檢測結果調查行業指南》(Guidance for Industry on Investigating OOS Test Results for Pharmaceutical Production)詳細說明了處理OOS的最佳實踐。
通過RTT實現過程控制和理解
在滿足當今生產需求的壓力下,許多公司正在采用PAT來提高運營效率和精益過程。RTT提供過程理解、過程控制、效率提升和優化,同時確保精確、準確和穩健的數據符合數據可靠性要求。
例如,在下圖中圈出的情況中,實時監控將提供做出實時決策所需的數據,并提供對污染源的洞察。如果TOC值和電導率值增加超出正常范圍,而無機碳水平保持在控制范圍內,則檸檬酸等污染物可能是罪魁禍首。借助經過驗證的準確數據,RTT為未來的工廠提供做出重要決策、實時排除故障并優化效率的能力。

關于作者

Kaitlyn Vap是Sievers分析儀生命科學產品應用專家,負責為Sievers總有機碳(TOC)分析儀的用戶提供技術支持。她與制藥行業公司合作,根據全球藥典監管標準使用Sievers的分析儀器對實驗室用水和藥品進行驗證。作為一名應用專家,她還探索和/或開發新的應用,以簡化水和藥品檢測流程。Kaitlyn擁有懷俄明大學化學工程學士學位。
◆?◆?◆
聯系我們,了解更多!
400?887 8280
sievers.china@suez.com
cn.sieversinstruments.com